HeLa ( / ˈ h iː l ɑː / ; also Hela or hela ) 是一種用於科學研究的永生化細胞系。它是最古老和最常用的人類細胞系。[1]該細胞係來源於1951 年 2 月 8 日採集的宮頸癌細胞,[2]來自Henrietta Lacks,一位 31 歲的非洲裔美國五個孩子的母親,她於 1951 年 10 月 4 日死於癌症,之後他們被命名為誰。[3]該細胞係被發現非常耐用且多產,這使其能夠廣泛用於科學研究。[4] [5]
萊克斯宮頸癌性腫瘤的細胞是在她不知情的情況下取出的,這在當時的美國很常見。[6] 細胞生物學家 George Otto Gey發現它們可以存活,[7]並開發了細胞系。以前,從其他人類細胞中培養出來的細胞只能存活幾天。來自拉克斯腫瘤的細胞表現不同。
歷史[編輯]
起源[編輯]
1951 年,一位名叫亨麗埃塔·拉克斯 (Henrietta Lacks)的患者因不規則陰道流血症狀被約翰霍普金斯醫院收治,隨後接受宮頸癌治療。[8]她的第一次治療是由小勞倫斯·沃頓 (Lawrence Wharton Jr.) 進行的,當時他未經她的同意從她的子宮頸採集了組織樣本。[9]她的宮頸活檢為組織培養實驗室負責人喬治·奧托·蓋伊 (George Otto Gey)的臨床評估和研究提供了組織樣本,就像其他外科手術所做的那樣。Gey 的實驗室助理 Mary Kubicek 使用滾管技術將細胞放入培養物中。[8]據觀察,這些細胞生長旺盛,每 20-24 小時翻一番,這與之前死亡的標本不同。[10]
在 1951 年萊克斯因癌症去世前不久,這些細胞由蓋伊繁殖。這是第一個在體外證明成功的人類細胞系,這是一項科學成就,對醫學研究具有深遠的未來益處。Gey 將這些細胞連同他的實驗室開發的工具和流程免費捐贈給任何出於科學利益而提出要求的科學家。拉克斯和她的家人都沒有允許採集細胞,但在那個時候,既不需要也不通常尋求許可。[11]這些細胞後來被商業化,但從未以其原始形式獲得專利。當時沒有要求將此類事項告知患者或其親屬,因為丟棄的材料或在手術、診斷或治療過程中獲得的材料是醫生或醫療機構的財產。
按照 Gey 實驗室助理的習慣,這種培養物以 Henrietta Lacks 名字和姓氏的前兩個字母命名。[8]在 1970 年代向公眾洩露她的真名之前,“HeLa”細胞係被錯誤地認為是以“Helen Lane”或“Helen Larson”命名的。[5] [12]
其他細胞培養物被可疑的 HeLa 細胞侵入,因此一個研究小組聯繫了 Lacks 家族,尋求 DNA 樣本以幫助識別污染細胞系。這家人一直不明白這次訪問的目的,但他們對研究人員告訴他們的事情的理解感到苦惱。[12] [13]這些細胞被視為癌細胞,因為它們來自宮頸可見病變的活組織檢查,作為拉克斯癌症診斷的一部分。[14]
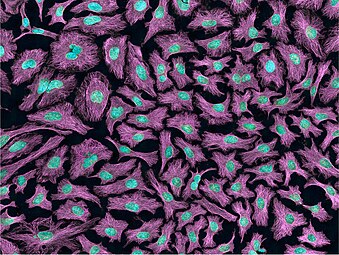
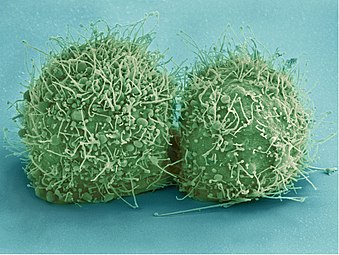
HeLa 細胞與其他細胞系一樣,被稱為“永生”,因為只要滿足基本的細胞存活條件(即在合適的環境中維持和維持),它們就可以在實驗室細胞培養板中無限次分裂。有許多HeLa 細胞株,因為它們在細胞培養物中不斷變異,但所有 HeLa 細胞都來自從 Lacks 中取出的相同腫瘤細胞。在細胞培養中增殖的海拉細胞總數遠遠超過海瑞塔·萊克斯體內的細胞總數。[15]
爭議[編輯]
萊克斯的案例是20 世紀醫學中缺乏知情同意的眾多例子之一。組織捐獻者和醫生之間幾乎不存在交流(即細胞是在未經患者同意的情況下獲取的,他們也沒有被告知這些細胞將用於什麼用途)。約翰霍普金斯醫院是巴爾的摩地區唯一一家非裔美國人患者可以免費接受治療的醫院,拉克斯接受治療並採集組織。從醫院的這個隔離部門接受免費治療的病人常常在他們不知情的情況下成為研究對象。[16]Lacks 的家人也無法訪問她的患者檔案,並且對於誰接受了 HeLa 細胞或它們將用於什麼用途沒有發言權。此外,隨著 HeLa 細胞在整個科學界的普及和使用越來越頻繁,Lacks 的親屬沒有獲得任何經濟利益,並且繼續生活在獲得醫療保健的機會有限的情況下。[17] [12]
誰擁有為研究而採集的組織樣本的問題在加州最高法院摩爾訴加州大學董事會案中被提出。法院裁定,一個人丟棄的組織和細胞不是他或她的財產,可以商業化。[18]
萊克斯的案例影響了 1981 年共同規則的製定。共同規則通過確保醫生告知患者是否計劃在研究中使用患者病例的任何細節並讓他們選擇是否披露細節來強制知情同意。與捐贈者姓名相關的組織也受此規則嚴格監管,樣本不再使用捐贈者姓名首字母命名,而是通過代碼編號命名。[18]為了進一步解決患者隱私問題,約翰·霍普金斯大學與美國國立衛生研究院和拉克斯的幾名家庭成員成立了一個聯合委員會,以確定誰可以訪問亨麗埃塔·拉克斯的基因組。[19]
2021 年,Henrietta Lacks 的遺產對Thermo Fisher Scientific涉嫌未經授權且廣為人知的 HeLa 細胞銷售行為提起訴訟,要求獲得過去和未來的付款。[20] Lacks 的家人聘請了一名律師,向 100 多家使用 HeLa 細胞並從中獲利的製藥公司尋求賠償。[21]
用於研究[編輯]
HeLa 細胞是第一個人類細胞,於 1953 年由丹佛科羅拉多大學的Theodore Puck和Philip I. Marcus成功克隆。[22]從那時起,HeLa 細胞“一直被用於研究癌症、艾滋病、輻射和有毒物質的影響、基因定位以及無數其他科學追求。” [23]根據作者Rebecca Skloot 的說法,到 2009 年,“已經發表了 60,000 多篇關於 HeLa 研究的科學文章,而且這個數字還在以每月 300 多篇的速度穩步增長。” [18]
根除小兒麻痺症[編輯]
1950 年代,Jonas Salk使用 HeLa 細胞來測試第一種脊髓灰質炎疫苗。他們被觀察到很容易感染脊髓灰質炎,導致感染細胞死亡。[2]這使得 HeLa 細胞非常適合用於脊髓灰質炎疫苗測試,因為結果很容易獲得。測試 Salk 的脊髓灰質炎疫苗需要大量的 HeLa 細胞,這促使國家小兒麻痺症基金會(NFIP) 尋找能夠大規模生產 HeLa 細胞的設施。[24] 1953年春,細胞培養工廠在塔斯基吉大學成立,為索爾克和其他實驗室提供海拉細胞。[25]不到一年後,索爾克的疫苗就可以進行人體試驗了。[26]
病毒學[編輯]
HeLa 細胞已被用於測試細小病毒如何感染人類、狗和貓的細胞。[27]這些細胞也被用於研究病毒,例如口鼻病毒(OROV)。OROV 導致培養細胞的破壞,細胞在被感染後不久開始退化,導致病毒誘導細胞凋亡。[28] HeLa 細胞已被用於研究乳頭瘤病毒E2的表達和細胞凋亡。[29] HeLa 細胞也被用於研究犬瘟熱病毒在癌細胞系中誘導細胞凋亡的能力, [30]這可能在開發對放射和化學療法具有抗性的腫瘤細胞的治療方法中發揮重要作用。[30]
HeLa 細胞還有助於開發人乳頭瘤病毒(HPV) 疫苗。在 1980 年代,Harald zur Hausen發現來自原始活組織檢查的 Lacks 細胞含有 HPV-18,後來發現它是導致 Henrietta Lacks 死亡的侵襲性癌症的原因。他在將 HPV 與宮頸癌聯繫起來方面的工作為他贏得了諾貝爾獎,並導致了 HPV 疫苗的開發,該疫苗預計可將宮頸癌死亡人數減少 70%。[31]
多年來,海拉細胞感染了包括 HIV、寨卡病毒、皰疹病毒和腮腺炎病毒在內的各種類型的病毒,以測試和開發新的疫苗和藥物。Richard Axel 博士發現,通過將 CD4 蛋白添加到 HeLa 細胞中,它們能夠感染 HIV,從而可以研究該病毒。[32] 1979 年,科學家了解到麻疹病毒在感染 HeLa 細胞時會不斷發生變異[33],並於 2019 年發現寨卡病毒無法在 HeLa 細胞中繁殖。[34]
巨蟹座[編輯]
HeLa 細胞已用於多項癌症研究,包括涉及性類固醇激素(如雌二醇、雌激素和雌激素受體)以及雌激素樣化合物(如槲皮素)及其抗癌特性的研究。[35]也有關於海拉細胞的研究,黃酮類化合物和抗氧化劑與雌二醇對癌細胞增殖的影響。
2011 年,HeLa 細胞被用於新型七次甲基染料IR-808 和其他類似物的測試,目前正在探索它們在醫學診斷、治療診斷學的發展、癌症患者藉助PDT的個體化治療等方面的獨特用途,co - 與其他藥物一起服用,並進行照射。[36] [37] HeLa 細胞已被用於涉及富勒烯的研究,以誘導細胞凋亡作為光動力療法的一部分,以及使用細胞系進行的體外癌症研究。[38]此外,HeLa 細胞還被用於定義 RNA 中的癌症標誌物,並被用於建立基於 RNAi 的識別系統和特定癌細胞的干擾。[39]
2014 年,HeLa 被證明是C57BL/6裸鼠腫瘤異種移植的活細胞系,[40]隨後被用於檢測氟西汀和順鉑對宮頸癌的 體內作用。
遺傳學[編輯]
1953 年,一個實驗室錯誤將 HeLa 細胞與錯誤的液體混合,這讓研究人員第一次能夠清楚地看到和計數他們所研究的 HeLa 細胞中的每條染色體。這一意外發現促使科學家Joe Hin Tjio和Albert Levan開發出更好的染色體染色和計數技術。[31]他們是第一個準確描述人類有 23 對染色體而不是以前認為的 24 對染色體的人。這對於研究涉及染色體數量的 唐氏綜合症等發育障礙非常重要。
1965 年,Henry Harris和 John Watkins 通過將 HeLa 細胞與小鼠胚胎細胞融合,創造了第一個人獸雜交種。這使得在將基因映射到特定染色體方面取得了進展,最終導致了人類基因組計劃。[31]
空間微生物學[編輯]
在 1960 年代,HeLa 細胞被送往蘇聯衛星Sputnik-6和人類太空任務,以確定太空旅行對活細胞和組織的長期影響。科學家發現,海拉細胞在零重力條件下分裂得更快。[41]
分析[編輯]
端粒酶[編輯]
HeLa細胞系衍生用於癌症研究。這些細胞增殖異常迅速,甚至與其他癌細胞相比也是如此。與許多其他癌細胞一樣,[42] HeLa 細胞在細胞分裂過程中具有活性端粒酶,[43]會一遍又一遍地複制端粒。這可以防止與衰老和最終細胞死亡有關的端粒逐漸縮短。通過這種方式,細胞繞過了Hayflick 極限,這是大多數正常細胞在衰老之前可以經歷的有限細胞分裂次數。結果是無限的細胞分裂和永生。
染色體數目[編輯]
從人乳頭瘤病毒 18 (HPV18) 到人宮頸細胞的水平基因轉移產生了 HeLa 基因組,它在許多方面都不同於 Henrietta Lacks 的基因組,包括其染色體數量。HeLa 細胞是快速分裂的癌細胞,在癌症形成和細胞培養過程中,染色體的數量會發生變化。目前的估計(不包括非常小的片段)是“超三倍體染色體數 (3n+)”,這意味著總染色體數為 76 到 80 條(而不是正常的二倍體數 46 條),其中有 22-25 條克隆異常染色體,稱為“HeLa 特徵染色體” ”。[44] [45] [46] [47]簽名染色體可以從多個原始染色體中派生出來,根據原始編號進行具有挑戰性的匯總計數。研究人員還注意到這些異常核型的穩定性。[44]結合光譜核型分析、FISH和傳統細胞遺傳學技術的研究表明,檢測到的染色體畸變可能代表晚期宮頸癌,並且可能存在於原發性腫瘤中,因為 HeLa 基因組即使在持續多年後仍保持穩定栽培。[44]
完整的基因組序列[編輯]
2013 年 3 月 11 日,在萊克斯家族不知情的情況下,對HeLa 細胞的完整基因組進行了測序並發表[48] [49] 。[50]家人提出了擔憂,因此作者自願拒絕訪問序列數據。[50] Jay Shendure在華盛頓大學領導了一個 HeLa 測序項目,該項目發表了一篇論文,該論文已於 2013 年 3 月被接受發表——但由於 Lacks 家族的隱私問題正在得到解決,該論文也被擱置了。[51] 2013年8月7日,美國國立衛生研究院院長弗朗西斯柯林斯根據與拉克斯家族三次會面後達成的協議,宣布了一項控制訪問細胞系基因組的政策。[52]數據訪問委員會將根據研究用於醫學研究的標準審查研究人員訪問基因組序列的請求,用戶將遵守 HeLa 基因組數據使用協議中的條款,其中包括所有 NIH-受資助的研究人員會將數據存入一個單一的數據庫以供將來共享。該委員會由六名成員組成,包括來自醫學、科學和生物倫理學領域的代表,以及萊克斯家族的兩名成員。[52]在一次採訪中,柯林斯讚揚了萊克斯一家願意參與到這種強加給他們的情況中。他將與他們的整個經歷描述為“強大的”,並說它以獨特的方式將“科學、科學歷史和倫理問題”結合在一起。[53]
污染[編輯]
HeLa 細胞有時難以控制,因為它們適應組織培養板中的生長,並具有侵入和勝過其他細胞系的能力。眾所周知,由於維護不當,它們會污染同一實驗室中的其他細胞培養物,干擾生物學研究並迫使研究人員宣布許多結果無效。HeLa 細胞在其他細胞類型中的污染程度是未知的,因為很少有研究人員測試已經建立的細胞系的身份或純度。已經證明,很大一部分體外細胞係被 HeLa 細胞污染;估計範圍從 10% 到 20%。這一觀察結果表明,任何細胞係都可能受到一定程度的污染。斯坦利·加特勒(1967) 和Walter Nelson-Rees (1975) 是第一個發表 HeLa 污染各種細胞系的人。[24] Gartler指出,“隨著細胞培養技術的不斷發展,幾乎可以肯定會發生種間和種內污染。” [8]
HeLa 細胞污染已成為一個普遍存在的世界性問題——甚至影響到包括Jonas Salk在內的許多著名醫生、科學家和研究人員的實驗室。海拉污染問題也加劇了冷戰緊張局勢。蘇聯和美國在理查德尼克松總統發起的抗癌戰爭中開始合作,卻發現交換的細胞被海拉污染。[54]
許多科學家和科普作家並沒有關注如何解決 HeLa 細胞污染問題,而是繼續將這個問題記錄為簡單的污染問題——不是由人為錯誤或缺陷引起的,而是由 HeLa 的堅韌、增殖或壓倒性特性引起的。[55]最近的數據表明,交叉污染仍然是現代細胞培養的主要持續問題。[4] [56]國際細胞系認證委員會 (ICLAC) 指出,許多細胞系錯誤鑑定的案例是培養物被另一種生長更快的細胞系交叉污染的結果。這讓人質疑使用受污染細胞系進行的研究的有效性,因為污染物的某些屬性可能來自完全不同的物種或組織,可能被錯誤地歸因於正在研究的細胞系。[57]
新物種提案[編輯]
HeLa 被進化生物學家 Leigh Van Valen描述為當代創造新物種的一個例子,被稱為Helacyton gartleri ,因為它們能夠無限複製,並且它們的染色體數量非人類。該物種以遺傳學家斯坦利·M·加特勒 (Stanley M. Gartler)的名字命名,範瓦倫 (van Valen) 稱讚他發現了“該物種的非凡成就”。[58]他對物種形成的論證基於以下幾點:
Van Valen 在同一篇論文中提出了新的 Helacytidae 科和Helacyton屬,並提出了 HeLa 細胞的新物種。[60]
然而,這一提議並沒有被其他著名的進化生物學家和其他學科的科學家認真對待。Van Valen 關於 HeLa 是一個新物種的論點不符合獨立的單細胞無性繁殖物種的標準,因為 HeLa 的核型眾所周知的不穩定性以及它們缺乏嚴格的祖先-後代譜系。[61]
畫廊[編輯]
在媒體[編輯]
- Adam Curtis於1997 年拍攝的紀錄片The Way of All Flesh解釋了 HeLa 的歷史及其對醫學和社會的影響。[62]
- 2010 年的法律與秩序“不朽”一集主要基於 Henrietta Lacks 和 HeLa 系列的故事,使用虛構的“NaRo”細胞作為替身。[63]
- HeLa 是Rebecca Skloot 2010 年出版的一本書《Henrietta Lacks 的不朽生命》的主題,該書調查了細胞系的歷史背景以及 Lacks 家族如何參與其使用。[12]
- 2017 年 HBO 電影《海瑞塔·拉克斯的不朽生命》就是根據這本書改編的。電影明星奧普拉·溫弗瑞、西爾維亞·格雷斯·克里姆、洛基·卡羅爾和蕾妮·愛麗絲·戈茲伯里飾演亨麗埃塔·拉克斯。作者麗貝卡·斯克魯特也作為角色出現在影片中,由蘿絲·拜恩飾演。[65]





沒有留言:
張貼留言
Love the Lord your God with all your heart and with all your soul and with all your mind.
耶 穌 對 他 說 : 你 要 盡 心 、 盡 性 、 盡 意 愛 主 ─ 你 的 神 。
—— Matthew 22:37 —— 馬 太 福 音 22:37